近日,我院李力教授团队在天然产物生物合成与合成生物学领域取得重要突破,相关研究成果以“Toward sustainable food preservatives: high-level production of sorbic acid in engineered Saccharomyces cerevisiae”为题,发表在国际权威期刊《Nature Communications》。该研究首次从微生物中完整解析了山梨酸的生物合成途径,并以酿酒酵母为底盘细胞构建了高效细胞工厂,实现了山梨酸的高水平生物合成,为食品防腐剂的绿色制造开辟了新路径。
山梨酸及其盐类是全球应用最广泛、最安全的食品防腐剂之一,被广泛用于食品、饮料及日化产品中,相关产业规模达数千亿美元。然而,目前山梨酸的工业化生产几乎完全依赖石油基化学合成路线,不仅消耗不可再生资源,而且面临环境负荷高、难以满足“天然来源”和“清洁标签”消费趋势等问题。开发绿色、可持续的山梨酸生物制造技术具有重要的科学意义与产业价值。
针对这一关键瓶颈,研究团队从植物病原真菌Myrothecium sp. FJNU6 中首次发现并分离出山梨酸及其酰胺衍生物,突破了该类化合物仅来源于植物的传统认知。通过全基因组测序与功能验证,团队成功解析了山梨酸的微生物生物合成途径,鉴定出由高还原型聚酮合酶(SoaA)、水解酶(SoaB)及酰胺转移酶(SoaC)构成的关键基因簇,并构建了仅依赖 SoaA 与 SoaB 的精简高效合成路径,从分子层面阐明了其生物合成机制。
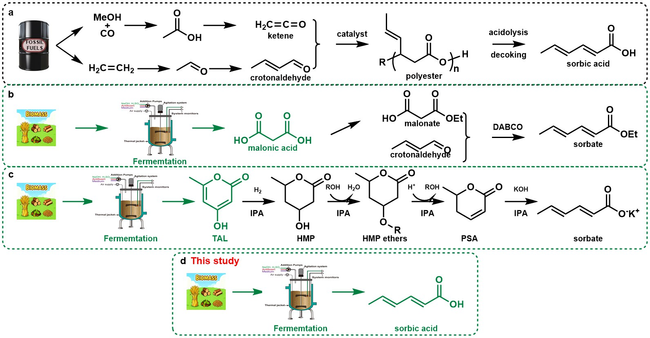
在此基础上,研究团队以食品级安全微生物——酿酒酵母为底盘细胞,开展了系统的代谢工程改造与发酵工艺优化。针对山梨酸对宿主细胞的毒性抑制问题,团队创新构建了动态调控表达系统,实现“生长—生产”阶段解耦;通过强化乙酰辅酶 A 与丙二酰辅酶 A 供给、优化碳代谢流分配,提高了关键前体的供应效率;进一步将合成通路区室化定位至过氧化物酶体,实现底物富集与毒性隔离,使产量提升约15倍。在工艺放大方面,团队建立了双阶段补料发酵策略,通过碳源利用与 pH 动态调控的协同优化,在50 L发酵罐中实现山梨酸产量1.84 g/L,创下目前酿酒酵母体系中山梨酸生物合成的最高水平,验证了其规模化生产的可行性。
该研究首次完整解析了山梨酸的微生物生物合成机制,搭建了从途径挖掘、底盘改造到过程优化的一体化全链条生物制造技术体系,为替代传统石油化工生产路线开辟了全新路径。研究成果既为食品防腐剂的绿色低碳制造夯实了核心技术根基,也为各类聚酮类天然产物的高效生物合成构建了可复制、可推广的通用技术范式。后续依托发酵工艺的持续迭代与生产成本优化,天然源山梨酸生物制造技术具备良好的产业化前景,有望推动食品工业的绿色低碳转型,助力健康产业高质量可持续发展。
我校为第一作者单位,我院2023级博士研究生萧建斌为第一作者,2022级博士研究生林威为共同第一作者,李力教授为通讯作者,张明亮老师与中国科学院大连化学物理研究所周雍进研究员为共同通讯作者。该工作得到国家重点研发计划、国家自然科学基金等项目的资助。
原文链接:https://doi.org/10.1038/s41467-026-72163-8